Углекислый газ CO2: от молекулы до газировки — всё о получении и применении
- Что такое углекислый газ: знакомство с молекулой
- Откуда берется углекислый газ: природные источники
- Получение углекислого газа в лабораторных условиях
- Промышленное производство углекислого газа
- Применение углекислого газа: от промышленности до быта
- Углекислый газ и экология: баланс между пользой и риском
- Часто задаваемые вопросы об углекислом газе
- Заключение
Каждый день вы выдыхаете его, пьёте в газировке, тушите им огонь и даже помогаете растениям расти. Углекислый газ — невидимый герой нашей жизни, о котором мы почти ничего не знаем. Откуда он берется? Как его получают на заводах и в лабораториях? Почему без него невозможна жизнь на Земле, но его избыток угрожает климату?
В этой статье — всё самое важное о CO2 простым языком, с примерами из жизни и объяснением химических процессов без сложных терминов.
Что такое углекислый газ: знакомство с молекулой
Углекислый газ, или двуокись углерода (химическая формула CO2), — это соединение одного атома углерода и двух атомов кислорода. В химии его также называют диоксидом углерода или оксидом углерода (IV). Представьте молекулу как три шарика, соединенных в линию: два красных (кислород) по краям и один черный (углерод) посередине.
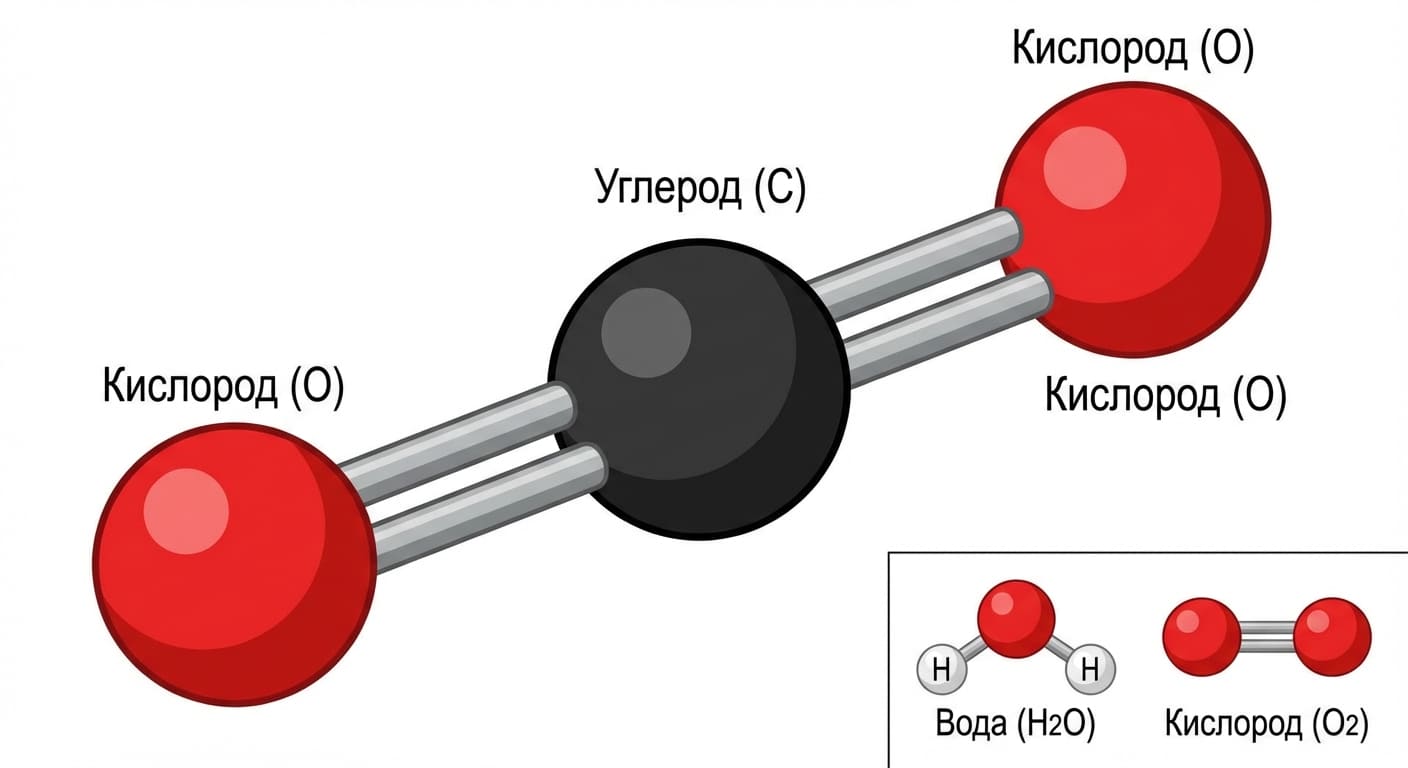
Основные свойства CO2
Углекислый газ при обычных условиях — это бесцветное вещество без запаха, которое тяжелее воздуха примерно в 1,5 раза. Именно поэтому он скапливается внизу помещений и может вытеснять кислород — об этом важно помнить при работе в подвалах или колодцах.
CO2 не горит и не поддерживает горение. Если внести горящую свечу в сосуд с углекислым газом, она сразу погаснет. Это свойство сделало диоксид углерода незаменимым в пожаротушении.
При температуре -78,5°C углекислый газ превращается в твердое вещество — сухой лёд, минуя жидкое состояние. Это называется сублимацией. Жидкий CO2 можно получить только под давлением.
Совет эксперта: При работе с углекислым газом в закрытых помещениях обязательно обеспечьте вентиляцию. Концентрация CO2 выше 5% вызывает головную боль и учащенное дыхание, а при 10% человек теряет сознание. Используйте датчики контроля атмосферы в помещениях, где хранятся баллоны с углекислотой.
Роль углекислого газа в природе
CO2 играет ключевую роль в двух важнейших процессах на Земле — фотосинтезе и дыхании. Растения поглощают углекислый газ из атмосферы и с помощью солнечного света превращают его в органические вещества, выделяя кислород. Животные и люди, наоборот, вдыхают кислород, а выдыхают CO2.
Углекислый газ также известен как парниковый газ. Он задерживает тепло в атмосфере Земли, создавая парниковый эффект. Без этого эффекта средняя температура на планете была бы около -18°C, и жизнь в привычной форме была бы невозможна. Проблема возникает, когда концентрация CO2 превышает естественный уровень.
Откуда берется углекислый газ: природные источники
Углекислый газ постоянно образуется в природе несколькими способами.
Дыхание живых организмов
Каждый раз, когда вы выдыхаете, в атмосферу попадает углекислый газ. В процессе дыхания организм расщепляет питательные вещества с помощью кислорода, получая энергию. Побочный продукт этого процесса — CO2, который выводится через легкие.
Средний человек выдыхает около 200-300 литров углекислого газа в сутки. Это примерно 1 кг CO2 в день. Если в комнате собирается много людей, концентрация диоксида углерода быстро растет — именно поэтому в душном помещении становится тяжело дышать и хочется открыть окно.
Разложение органических веществ
Когда опавшие листья, упавшие деревья или останки животных разлагаются, бактерии и грибы расщепляют органику, выделяя углекислый газ. Этот процесс возвращает углерод, накопленный растениями, обратно в атмосферу.
Вулканическая деятельность
Вулканы выбрасывают огромное количество CO2 из недр Земли. Углекислый газ содержится в магме и высвобождается при извержениях. Некоторые вулканические озера и минеральные источники насыщены углекислотой — такая вода становится естественно газированной.

Горение и окисление
При горении любого углеродсодержащего вещества — дерева, угля, нефтепродуктов — образуется углекислый газ. Химическая реакция выглядит так:
C + O₂ → CO₂
Углерод соединяется с кислородом из воздуха, образуя диоксид углерода. Именно поэтому костры и двигатели автомобилей — источники CO2.
Получение углекислого газа в лабораторных условиях
В школьной или домашней лаборатории углекислый газ получают несколькими простыми способами.
Реакция соды с уксусом
Это самый доступный способ получить CO2 дома. Когда пищевая сода (гидрокарбонат натрия) взаимодействует с уксусной кислотой, происходит бурная реакция с выделением углекислого газа:
NaHCO₃ + CH₃COOH → CH₃COONa + H₂O + CO₂↑
Вы сразу увидите "шипение" и пузырьки газа. Если поднести к отверстию сосуда горящую спичку, она погаснет — CO2 вытеснил кислород.
Действие кислот на карбонаты
Классический школьный эксперимент — взаимодействие мела или мрамора (карбонат кальция) с соляной кислотой:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑
Кусочек мела помещают в пробирку с кислотой, и начинается выделение газа. Его собирают в перевернутый стакан или пропускают через известковую воду, которая мутнеет — это доказывает присутствие углекислого газа.

Разложение карбонатов при нагревании
При сильном нагревании карбонаты распадаются на оксид металла и углекислый газ:
CaCO₃ → CaO + CO₂↑
Эта реакция происходит при температуре выше 900°C. Именно так получают негашеную известь (оксид кальция) в промышленности, попутно выделяя большое количество CO2.
Безопасность: При проведении опытов с кислотами работайте в перчатках и защитных очках. Не наклоняйтесь над сосудом с реакцией. Проветривайте помещение, так как высокая концентрация углекислого газа опасна.
Промышленное производство углекислого газа
Углекислый газ занимает около 10% рынка технических газов и производится в огромных объемах для различных отраслей промышленности. Промышленные методы получения CO2 гораздо более масштабны, чем лабораторные.
Получение из дымовых газов предприятий
Основной источник промышленного CO2 — дымовые газы тепловых электростанций, цементных заводов и металлургических производств. При сжигании угля, газа или мазута образуется смесь газов, содержащая 10-15% углекислого газа.
Из дымовых газов CO2 извлекают методами абсорбции — пропускают через специальные растворы (например, моноэтаноламин), которые поглощают диоксид углерода. Затем раствор нагревают, и чистый CO2 высвобождается. После очистки и сжижения его закачивают в баллоны или резервуары.
Компания "Айр Техник" поставляет углекислый газ высокой чистоты для различных отраслей промышленности. Посмотреть каталог технических газов можно на сайте https://airtechnik.ru.
Производство при обжиге известняка
При производстве цемента и извести известняк (карбонат кальция) обжигают при высокой температуре. В результате разложения выделяется огромное количество углекислого газа — около 0,5 тонны CO2 на тонну извести.
Этот побочный продукт собирают, очищают и используют в промышленности. Такой способ делает производство CO2 экономически выгодным, так как газ получается практически бесплатно.
Брожение в пищевой промышленности
При производстве пива, вина и спирта происходит процесс брожения — дрожжи перерабатывают сахар в спирт и углекислый газ:
C₆H₁₂O₆ → 2C₂H₅OH + 2CO₂↑
На крупных пивоварнях и спиртзаводах устанавливают системы улавливания CO2. Газ очищают, сжимают и используют для газирования напитков или продают другим предприятиям. Это пример замкнутого цикла производства.
Синтез аммиака и другие химические процессы
В химической промышленности углекислый газ образуется как побочный продукт при производстве аммиака, водорода и других веществ. Эти источники дают CO2 высокой чистоты, который особенно ценится в медицине и пищевой промышленности.
Хранение и транспортировка CO2
Углекислый газ хранят в трех основных формах:
- Сжатый газ — в баллонах под давлением 150-200 атмосфер. Баллоны окрашены в черный цвет с желтой надписью "CO2".
- Жидкий CO2 — в изотермических резервуарах при температуре около -20°C и давлении 20 атмосфер. Так транспортируют большие объемы газа.
- Сухой лёд — твердая форма, которую получают при резком расширении жидкого CO2. Температура сухого льда -78,5°C.

Применение углекислого газа: от промышленности до быта
Диоксид углерода находит применение практически во всех отраслях экономики. Рассмотрим основные направления использования этого универсального газа.
Пищевая промышленность
Газирование напитков — самое известное применение CO2. Углекислый газ под давлением растворяют в воде, лимонаде, пиве или квасе. При открывании бутылки давление падает, и газ выходит в виде пузырьков. В одной бутылке газировки объемом 0,5 литра содержится около 4-5 граммов углекислого газа.
Процесс насыщения жидкости углекислотой называется карбонизацией. В промышленности используют специальные сатураторы — устройства, где вода и CO2 смешиваются под давлением 3-4 атмосферы.
Консервирование и упаковка продуктов — углекислый газ создает защитную атмосферу, которая замедляет окисление и размножение бактерий. Свежее мясо, рыбу, салаты упаковывают в контейнеры, заполненные смесью CO2 и азота. Это продлевает срок хранения в несколько раз без консервантов.
Заморозка продуктов — жидкий CO2 и сухой лёд используют для быстрой ("шоковой") заморозки. При температуре -78°C продукт замерзает за считанные минуты, сохраняя структуру клеток и вкусовые качества.
Для предприятий пищевой промышленности "Айр Техник" предлагает углекислый газ пищевой чистоты с сертификатами качества. Подробности о поставках CO2 для газирования и консервирования — на сайте компании.
Сельское хозяйство и растениеводство
В теплицах углекислый газ подают для подкормки растений. При повышении концентрации CO2 до 0,1-0,15% (в 3-4 раза выше естественного уровня) фотосинтез ускоряется, и урожайность возрастает на 20-40%.
Систему подачи углекислоты монтируют вдоль грядок. Газ тяжелее воздуха и опускается к листьям растений. Особенно эффективна подкормка CO2 для томатов, огурцов, зелени и цветов.
В аквариумистике углекислый газ подают для стимуляции роста водных растений. Специальные баллоны с редуктором и диффузором создают оптимальную концентрацию CO2 в воде — около 20-30 мг/л.
Пожаротушение
Углеродные огнетушители работают на простом принципе: CO2 вытесняет кислород и охлаждает горящую поверхность. Газ подается под высоким давлением, образуя облако "снега" из мелких кристаллов сухого льда.
Углекислотные огнетушители незаменимы там, где нельзя использовать воду или пену — в серверных, архивах, музеях, на электроустановках. После применения CO2 не оставляет следов и не портит оборудование.
Стационарные системы пожаротушения на основе углекислого газа устанавливают в машинных залах, покрасочных камерах, складах ГСМ. При срабатывании системы помещение заполняется CO2, концентрация кислорода падает ниже 15%, и горение прекращается.

Совет эксперта: При использовании углекислотного огнетушителя не беритесь за раструб голыми руками — он охлаждается до -70°C и может вызвать обморожение. Держите огнетушитель за пластиковую ручку. После применения CO2-системы в помещении обязательно проветрите комнату перед входом людей.
Медицина
В медицине углекислый газ применяется в нескольких направлениях:
Лапароскопические операции — хирурги заполняют CO2 брюшную полость пациента, создавая рабочее пространство для инструментов. Углекислый газ быстро всасывается тканями и безопасен для организма.
CO2-лазеры — используются в косметологии и хирургии для удаления новообразований, шлифовки кожи и бескровных операций. Лазер на углекислом газе генерирует мощный инфракрасный луч, который испаряет ткани.
Стимуляция дыхания — смесь кислорода с 5-7% углекислого газа (карбоген) применяют для стимуляции дыхательного центра при отравлениях, асфиксии и в реанимации.
Карбокситерапия — инъекции медицинского CO2 под кожу улучшают кровообращение, стимулируют обмен веществ и используются в косметологии для омоложения.
Химическая промышленность
Углекислый газ — важное сырье для химического синтеза:
Производство соды (карбоната натрия) — CO2 пропускают через раствор соли и аммиака. Сода используется в производстве стекла, моющих средств и бумаги.
Синтез мочевины — главного азотного удобрения. Углекислый газ реагирует с аммиаком при высоком давлении и температуре.
Производство метанола — перспективное направление химии. CO2 восстанавливают водородом, получая метиловый спирт — топливо и сырье для пластиков.
Охлаждение и заморозка: сухой лёд
Сухой лёд — это твердый углекислый газ при температуре -78,5°C. Он получается при резком расширении жидкого CO2 — часть газа превращается в белый "снег", который прессуют в брикеты или гранулы.
Преимущество сухого льда — он не тает, а сублимирует (переходит из твердого состояния сразу в газ), не оставляя воды. Это делает его идеальным хладагентом для транспортировки:
- Мороженого и замороженных продуктов
- Медицинских препаратов и вакцин
- Биологических образцов
- Скоропортящихся грузов
В медицине сухой лёд используют для хранения тканей и органов при температуре ниже -70°C. В научных лабораториях — для охлаждения реакций и создания криогенных ловушек.
Бластинг сухим льдом — современная технология очистки поверхностей. Гранулы сухого льда подают под давлением на загрязненную поверхность. CO2 охлаждает и разрушает загрязнения, а затем испаряется. Метод не оставляет отходов и не повреждает основу. Применяется для очистки оборудования, удаления краски, формовой смазки и других загрязнений.

Нефтяная промышленность
В нефтедобыче углекислый газ закачивают в истощенные скважины для вытеснения остатков нефти. CO2 под давлением растворяется в нефти, снижает ее вязкость и выталкивает к скважине. Это увеличивает нефтеотдачу пласта на 10-20%.
Также диоксид углерода используют для интенсификации добычи — при закачке в скважину жидкого CO2 происходит резкое расширение газа, которое разрушает породу и улучшает проницаемость пласта.
Сварка и металлообработка
В сварочном производстве углекислый газ применяют как защитную среду при полуавтоматической сварке. CO2 вытесняет воздух из зоны сварки, предотвращая окисление металла. Сварка в среде углекислого газа дешевле, чем в аргоне, и подходит для стали.
Часто используют смесь CO2 с аргоном (обычно 80% аргона и 20% CO2) — это улучшает качество шва и стабильность дуги.
Развлечения и спецэффекты
Сухой лёд создает эффектный густой белый "туман", который стелется по полу. Это происходит потому, что холодный CO2 конденсирует водяной пар из воздуха, образуя облако мелких капелек.
Эффект используют:
- На концертах и в театрах для создания атмосферы
- В ночных клубах на "пенных вечеринках"
- При оформлении праздников и фотосессий
- В ресторанах для эффектной подачи блюд
"Айр Техник" поставляет углекислый газ и сухой лёд для различных мероприятий. Широкий ассортимент баллонов и форм упаковки CO2 — от лабораторных до промышленных объемов.
Углекислый газ и экология: баланс между пользой и риском
Углекислый газ играет двойственную роль в современном мире. С одной стороны, он абсолютно необходим для жизни на Земле. С другой — избыточные выбросы CO2 от деятельности человека приводят к изменению климата.
Парниковый эффект и климат
Естественная концентрация CO2 в атмосфере — около 0,04% (400 ppm). Этот уровень поддерживался тысячелетиями за счет баланса между выделением и поглощением углекислого газа.
С начала промышленной революции концентрация выросла до 0,042% (420 ppm) и продолжает увеличиваться. Основные источники антропогенного CO2:
- Сжигание ископаемого топлива (уголь, нефть, газ)
- Вырубка лесов
- Производство цемента
- Промышленные процессы
Рост концентрации углекислого газа усиливает парниковый эффект — больше тепла задерживается в атмосфере. Это приводит к повышению средней температуры Земли, таянию ледников, изменению климатических зон.
Технологии улавливания и хранения CO2
Для снижения выбросов разрабатываются технологии улавливания углекислого газа (CCS — Carbon Capture and Storage). Суть метода: CO2 извлекают из дымовых газов предприятий, сжимают и закачивают в глубокие геологические формации — истощенные месторождения нефти и газа или соленосные водоносные горизонты.
Перспективное направление — использование уловленного CO2 как сырья для химической промышленности. Вместо того чтобы хранить газ под землей, его превращают в полезные продукты — топливо, пластики, строительные материалы.
Совет эксперта: Предприятия, которые внедряют системы улавливания CO2, не только снижают экологический след, но и получают дополнительный источник дохода. Уловленный углекислый газ можно продать для пищевой промышленности, сельского хозяйства или нефтедобычи. Это превращает отход в ценный продукт.
Баланс: необходимость и ответственность
Углекислый газ — это не "враг", а неотъемлемая часть жизни на Земле. Проблема не в самом CO2, а в нарушении естественного баланса его круговорота. Растения, океаны и почвы поглощают около половины выбросов, но остальная часть накапливается в атмосфере.
Ответственное отношение к использованию углекислого газа означает:
- Повышение энергоэффективности и переход на возобновляемые источники энергии
- Внедрение технологий улавливания и повторного использования CO2
- Лесовосстановление и защита природных поглотителей углерода
- Осознанное потребление и сокращение углеродного следа
Часто задаваемые вопросы об углекислом газе
Чем опасен углекислый газ для человека?
При концентрации выше 1% CO2 вызывает сонливость и головную боль. При 5% — учащенное дыхание и сердцебиение. При 10% и выше — потерю сознания. Смертельная концентрация — около 20-30%. Опасность представляют закрытые помещения без вентиляции, где может скапливаться тяжелый углекислый газ — подвалы, колодцы, емкости. При работе с баллонами CO2 обеспечьте проветривание и используйте датчики контроля атмосферы.
Можно ли хранить баллон с углекислым газом дома?
Баллоны с CO2 можно хранить дома, соблюдая правила безопасности. Держите баллон в вертикальном положении, вдали от источников тепла и прямых солнечных лучей. Температура хранения — не выше +40°C. Обеспечьте вентиляцию помещения. Не допускайте ударов по баллону и падений. Проверяйте состояние вентиля и редуктора. Для бытовых нужд (газирование воды, аквариумы) используйте небольшие баллоны объемом 1-5 литров.
Как получить углекислый газ в домашних условиях?
Простейший способ — смешать пищевую соду с уксусом. На 1 столовую ложку соды добавьте 50-100 мл уксуса. Реакция начнется мгновенно с выделением CO2. Такой метод подходит для простых экспериментов. Для постоянного использования (например, для аквариума) удобнее купить баллон с углекислым газом и редуктором — это безопаснее и экономичнее.
Почему газировка "шипит" при открывании?
В закрытой бутылке углекислый газ растворен в жидкости под давлением 3-4 атмосферы. При открывании крышки давление падает до атмосферного, и газ начинает выходить из раствора в виде пузырьков. Чем выше было давление и ниже температура напитка, тем больше CO2 было растворено, и тем "газированнее" напиток. Тепло ускоряет выход газа — поэтому теплая газировка "выдыхается" быстрее холодной.
Заключение
Углекислый газ — удивительное вещество, которое окружает нас повсюду, хотя мы его не видим. Это и основа фотосинтеза, и компонент газировки, и эффективное средство пожаротушения, и важное сырье для промышленности.
CO2 получают из природных источников и как побочный продукт промышленных процессов. Современные технологии позволяют улавливать углекислый газ из дымовых труб и превращать его в полезные продукты — от сухого льда до химического сырья.
Применение диоксида углерода простирается от пищевой промышленности до космических технологий, от медицины до развлечений. Этот газ демонстрирует, как одно простое вещество может находить применение в совершенно разных областях благодаря своим уникальным свойствам.
Ключ к успешному использованию CO2 — понимание его природы и соблюдение баланса. Углекислый газ необходим для жизни, но его избыток создает проблемы. Ответственное отношение к производству и использованию CO2 поможет сохранить этот баланс.
Теперь, когда вы открываете бутылку газировки или видите огнетушитель, вы знаете — это работа удивительной молекулы CO2, невидимого героя нашей повседневной жизни.
Компания "Айр Техник" — ваш надежный поставщик технических газов. Углекислый газ различной чистоты, сухой лёд, баллоны и оборудование для газоснабжения. Более 10 лет опыта на рынке промышленных газов.
Статья подготовлена специалистами "Айр Техник" на основе многолетнего опыта работы с техническими газами и современных научных данных.
Чтобы уточнить стоимость или получить дополнительную консультацию,
вы можете позвонить по тел.: +7 (495) 545-44-62 или отправить запрос.
